| Stadium | Definition |
| I |
|
| IIA | Retroperitoneale Lymphknotenmetastasen < 2cm |
| IIB | Retroperitoneale Lymphknotenmetastasen 2.1-5 cm |
| IIC | Retroperitoneale Lymphknotenmetastasen > 5cm |
| IIIA | Supraclavikuläre oder mediastinale Metastasen |
| IIIB | Lungenmetastasen: Minimal: < 5 Metastasen in jedem Lappen, aber < 2 cm fortgeschritten: >5 Metastasen in jedem Lappen oder 1 Läsion > 2cm |
| IIIC | Extrapulmonale Metastasen |
- Startseite
- Erkrankungen & Therapien
- Hodentumor
- Diagnostik des Hodentumors
Diagnostik des Hodentumors
Der typische Leitbefund eines Hodentumors ist die schmerzlose Hodenvergrößerung, die entweder selbst getastet wird oder durch ein Schweregefühl des tumortragenden Hodens auffällt. Die Diagnose wird erhärtet durch die Sonografie beider Hoden sowie durch die Bestimmung der Tumormarker alfa-Fetoprotein (AFP), humanes ß-Choriogonadotropin (ß-hCG) und die Laktatdehydrogenase (LDH) im Blut.
Zur Diagnosesicherung erforderlich ist die operative Exploration des Hodens über einen Leistenschnitt. Besteht kein Zweifel am Vorliegen eines bösartigen Hodentumors, wird der tumortragende Hoden bei gesundem Gegenhoden komplett entfernt. Gegebenenfalls kann aus kosmetischen Gründen in gleicher Sitzung eine Prothese in das Hodenfach eingelegt werden.
Ist präoperativ unklar, ob ein bösartiger oder gutartiger Hodentumor vorliegt, wird der Tumor enukleiert und der sogenannten Schnellschnittuntersuchung zugeführt. Bei gutartigem Befund kann der Hoden belassen werden, bei malignem Befund muss dieser entfernt werden. Wie wir in eigenen Untersuchungen haben zeigen können, ist die Schnellschnittuntersuchung in erfahrenen Händen absolut zuverlässig. Die Fehlerrate in der Beurteilung „bösartig versus gutartig“ liegt in den erfahrenen Zentren bei < 1%.
Die Entnahme einer Gewebeprobe des vermeintlich nicht betroffenen Gegenhodens zum Ausschluss von sogenannten Vorläuferzellen (Carcinoma-in-situ, testikuläre intraepitheliale Neoplasie) sollte bei Vorliegen von Risikofaktoren (Hodenvolumen < 12ml, Alter < 30 Jahre, Fertilitätsstörungen) bei einem Risiko von ca. 34% immer erfolgen. Hierbei ist eine Probe vom Ober- sowie vom Unterpol des Hodens zu entnehmen und in einer speziellen Fixierungslösung (Bouin’sche Lösung) dem Pathologen zuzusenden, der obligatorisch eine immunhistochemische Färbung gegen die auf der Zelloberfläche exprimierten plazentaren alkalischen Phosphastase vornimmt, um die TIN-Zellen sicher zu identifizieren.
Liegt zeitgleich oder zeitversetzt zum Primärtumor ein beidseitiger Hodentumor vor, sollte entsprechend der Leitlinien ein organerhaltendes Vorgehen in erfahrenen Zentren vorgenommen werden. Dieses von unserer Arbeitsgruppe erstmals 1994 beschriebene Therapiekonzept erhält die körpereigene Hormonproduktion bei über 80% der Patienten im Langzeitverlauf und ist nicht mit einem erhöhten Risiko eines Lokalrezidivs verbunden (siehe unten). Nach der organerhaltenden Enukleation des Tumors sollte der Resthoden jedoch einer Bestrahlung zugeführt werden, um die im Resthoden immer vorkommenden Vorläuferzellen eliminieren zu.
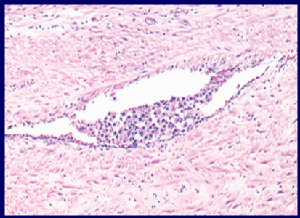
Nach Entfernung des tumortragenden Hodens wird dieser entsprechend der Empfehlungen der WHO genauestens mikroskopisch analysiert, um alle feingeweblichen Subtypen der testikulären Keimzelltumoren identifizieren zu können. Ebenso muss das Vorliegen einer vaskulären Invasion (Abbildung 4) beschrieben oder definitiv ausgeschlossen werden. Diese Informationen sind für die spätere Therapieplanung wichtig, da beispielsweise ein hoher Anteil an embryonalem Karzinom in Kombination mit einer vaskulären Invasion im klinischen Stadium I eines nichtseminomatösen KZT (siehe unten) mit einer hohen Rate mikroskopischer Lymphknotenmetastasen assoziiert ist und die Option einer adjuvanten Therapie eröffnet.
Stagingdiagnostik
Ist der maligne KZT histologisch gesichert, muss eine Umfelddiagnostik zum Ausschluss von Metastasen eingeleitet werden. Hierzu wird in aller Regel eine Computertomografie (CT) des Thorax, des Abdomens und des kleinen Beckens durchgeführt. Die Befundung insbesondere des CT der hinteren Bauchregion (Retroperitoneum) sollte immer gemeinsam durch den Urologen und Radiologen erfolgen und die primären Lymphabflussstationen des Hodens berücksichtigen. So findet sich die primäre Lymphknotenstation eines rechtsseitigen Hodentumors in der interaortocavalen Region und diejenige eines linksseitigen Hodentumors in der präaortalen bzw. paraaortalen Region jeweils in Höhe der Nierengefäße. Zur adäquaten Beurteilung der Lymphknoten ist es immer erforderlich, den transversalen und den longitudinalen Durchmesser der Lymphknoten zu bestimmen: ein Längsdurchmesser von 1cm in der primären Lymphabflusszone bei entsprechenden Risikofaktoren im Primärtumor ist fast immer mit einer Mikrometastasierung assoziiert und bedarf einer entsprechenden Therapie. Eine Kernspintomografie des Bauchraumes führt gegenüber dem CT nicht zu einer besseren Aussagekraft, ist jedoch aufgrund der fehlenden Strahlenbelastung gerade in der Nachsorge zu bevorzugen. Die Positronenemissionstomografie (PET/CT) spielt in der primären Diagnostik keine Rolle.
Der halbwertszeitgerechte Abfall der Tumormarker AFP (Halbwertszeit: 5-7 Tage) und ß-hCG (Halbwertszeit: 24-36 Stunden) sowie deren absolute Höhe nach Ablatio testis bestimmen in Zusammenschau mit den Befunden der bildgebenden Umfelddiagnostik die weitere Prognose und die individuell sinnvollste Therapie. Ein nicht halbwertszeitgerechter Abfall oder eine Plateaubidung unter Therapie spricht für eine ungünstige Prognose und macht eine frühzeitige Umstellung der Therapie erforderlich.
Basierend auf der Höhe der Tumormarker und der Ausdehnung sowie Lokalisation möglicher Metastasen erfolgt die klinische Stadieneinteilung nach der Lugano-Klassifikation (Tabelle 1) bzw. der Klassifikation der International Germ Cell Cancer Consensus Group (IGCCCG, Tabelle 2). Die IGCCCG-Klassifikation ist die bei fortgeschrittener Metastasierung eingesetzte Klassifikation und bestimmt die Intensität der systemischen Therapie.
Tabelle 1: Lugano-Klassifikation; beachte: ab Stadium IIC wird zur Prognosebeurteilung und Therapieplanung die IGCCCG-Klassifikation verwendet
| Prognose | Seminom | Nichtseminom |
| Günstig Heilungsrate: 95% | Jede Primärlokalisation Keine nichtpulmonalen viszeralen Metastasen AFP negativ ß-hCG < 1.000 ng/ml LDH < 1.5fach der Norm | testikuläre oder retroperitoneale extragonadale Primärlokalisation Keine nichtpulmonalen viszeralen Metastasen AFP < 1.000 ng/ml ß-hCG < 1.000 ng/ml LDH < 1.5fach der Norm |
| intermediär Heilungsrate: 70% | Jede Primärlokalisation extrapulmonale viszerale Metastasen | Primärlokalisation: Hoden, extragonadal retroperitoneal Keine nichtpulmonalen viszeralen Metastasen |
| AFP 1.000 – 10.000 ng/ml ß-hCG 1.000 – 10.000 ng/ml LDH 1.5 – 10fch der Norm | AFP 1.000 – 10.000 ng/ml ß-hCG 1.000 – 10.000 ng/ml LDH 1.5 – 10fch der Norm | |
| Ungünstig Heilungsrate: 50% | Primär mediastinaler KZT Extrapulmonale viszerale Metastasen AFP > 10.000 ß-hCG > 10.000 LDH > 10fach der Norm |
Tabelle 2: IGCCCG-Klassifikation