- Startseite
- Erkrankungen & Therapien
- Prostatakrebs
- Kastrationsresistentes Prostatakarzinom (KRPCA)
Kastrationsresistentes Prostatakarzinom (KRPCA)
Das kastrationsresistente Prostatakarzinom (KRPCA) wird definiert durch einen dreimalig nachgewiesenen konsekutiven PSA-Anstieg im wöchentlichen Abstand nach primärer Hormontherapie trotz im Kastrationsbereich gelegener Testosteronserumspiegel oder ein radiologischer Progress von Knochen oder Weichteilmetastasen. Der festgelegte Testosteronspiegel liegt bei 50 ng/dl. Dies geht auf ältere Studien zurück. Mittlerweile konnte gezeigt werden, dass das progressionsfreie Überleben im Falle von niedrigeren Testosteronwerten (<20ng/dl) verlängert ist, so dass dem Testosteronwert unter der Hormonentzugstherapie besonderes Augenmerk gilt. Die früher erforderliche sekundäre Hormontherapie wurde aus der Definition genommen. Klinisch wird das KRPCA dominiert durch Knochenmetastasen, die zu Schmerzen, pathologischen Frakturen, Gewichtsverlust, spinaler Kompression bis hin zu einem Querschnitt Anämie, Thrombozytopenie und einer signifikanten Reduktion des körperlichen Allgemeinzustands führen können.
Therapie
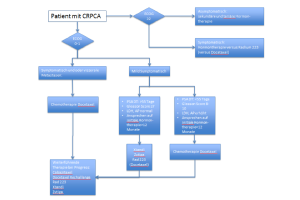
Für die Therapie des KRPKA gibt es verschiedene Ansätze. Die für den Patienten idealerweise eingesetzte primäre Therapie wird anhand von verschiedenen patientenspezifischen- und Laborparametern erarbeitet. Dies sind insbesondere der Allgemeinzustand des Patienten, in der Regel als sogenannter ECOG Performance Status bezeichnet, der Schmerzstatus, PSA Dynamik und weitere Faktoren wie alkalische Phosphatase, LDH und Metastasenlast. Als Orientierung dient der unten in der Datei dargestellte Algorithmus. Für die Therapie sollten die folgenden Faktoren berücksichtigt werden:
- Symptomatik
- Nebenwirkungen der Therapieoptionen
- Patientenpräferenz
- Komorbidität, Lebenserwartung und Lebensqualität
- Progressionsdynamik
- Lokalisation von Metastasen und generelle Tumorlast.
Für die Therapie des kastrationsresistenten Prostatakarzinoms stehen aktuell mehrere Präparate zur Verfügung. Bei unterschiedlichen Therapieansätzen sind diese für verschiedene Indikationsstellung aber insbesondere mit unterschiedlichen Nebenwirkungen verbunden. Eine Unterteilung der Präparate kann in zytotoxische, antihormonell und in Radionuklide erfolgen.
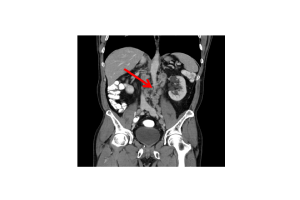
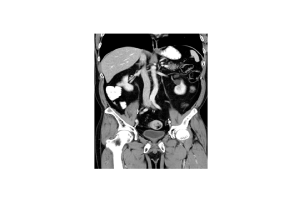
Docetaxel
Docetaxel ist ein Hemmer des Mikrotubuli-Systems und führt somit in der Zellteilung zu einem sogenannten Zellarrest und Untergang der Zellen. Es war das erste Präparat welches bei Patienten mit einem früher als hormonrefraktär beschriebenen Tumorstadium in verschiedenen klinischen Studien einen Überlebensvorteil bringen konnte. Die klinische Einführung erfolgte 2005. Die übliche Dosierung ist die Applikation von 75 mg/m² KOF alle 3 Wochen in Kombination mit Prednison, 2 x 5 mg/die. Gerade beim symptomatischen CRPCA ist die primäre Chemotherapie die primäre Therapieempfehlung bei Patienten mit einem guten Allgemeinzustand.
Die Behandlung mit Docetaxel sollte über 6 Zyklen geplant werden und kann in Abhängigkeit vom Ansprechen und vom Nebenwirkungsprofil auf 10 Zyklen ausgedehnt werden. Bei der initialen Bewertung des therapeutischen Ansprechens ist das PSA-Flare-up-Phänomen als Zeichen einer verstärkten Apoptose des PCA zu berücksichtigen, das bei 15-20 % der Patienten während der ersten 3 Zyklen auftreten kann und sich durch einen kontinuierlichen PSA-Anstieg mit nachfolgender PSA-Regression manifestiert. PSA-Verläufe während der ersten 3 Zyklen sollten somit keinen Einfluss auf die Fortsetzung der Therapie ausüben. Die Empfehlung der Prostate Cancer Working Group 2 spricht bei allen Therapieoptionen eine Applikation über 3 Monate aus, bevor ein Abbruch der Therapie in Erwägung gezogen werden sollte.
Als Nebenwirkungen sind besonders zu berücksichtigen die Hämatotoxizität mit einer febrilen Neutropenie als onkologischer Notfall in 4%, neurologische Störungen zwischen 6% und 25% und gastroenterologischen Nebenwirkungen zwischen 13% und 37%. Reversible Nagelveränderungen und Haarverlust unter der Therapie werden in 9% und 39% angegeben. Unter einer Änderung des Therapieregimes auf 2 wöchentliche Applikationen mit einer Dosierung mit 50mg/m2 KOF konnte eine signifikante Reduktion der Nebenwirkungen erreicht werden. Eine Umstellung der Dosierung kann bei initial schlechter Verträglichkeit oder im Falle einer Re-Challenge erfolgen.
Cabazitaxel
Nachdem verschiedene Kombinationstherapien mit Docetaxel keinen Benefit bzgl. des onkologischen Outcomes erbrachten, konnte mit der Entwicklung von Cabazitaxel eine weitere Chemotherapie mit signifikantem Überlebensvorteil bei Patienten nach primärer Chemotherapie im Vergleich zur früher etablierten Therapie mit Mitoxantron in einer Phase III Studie zugelassen werden. Cabazitaxel ist ein synthetisches Taxan welches zunächst in Docetaxel resistenten Zelllinien einen Effekt gezeigt hat, welcher dann in die Klinik übertragen werden konnte. Die in der Zulassungsstudie beschriebenen Grad-3/4-Toxizitäten mit Neutropenien (81,7 %), Anämien (10,5 %), febrile Neutropenien (7 %) und Diarrhoen (6,2 %) konnten weder im Härtefallprogramm nach Zulassung noch in Folgestudien (Firstana und Proselica) bestätigt werden. Eine Dosisreduktion von 25mg/m2 KOF auf 20mg/m2 KOF führt zu einer Reduktion der hämatotoxischen Nebenwirkungen ohne den onkologischen Effekt negativ zu beeinflussen. Bei beiden Dosierungen stehen die neurologischen Nebenwirkungen mit Parästhesien (Taubheitsgefühlen) in Händen und Füßen im Hintergrund. Schwerwiegende Ereignisse werden unter der Therapie nicht beschrieben. Insgesamt ist die subjektive Belastung der Patienten unter Cabazitaxel im Vergleich zu Docetaxel deutlich geringer angegeben.
Abiraterone
Abirateronazetat (AA) hemmt ein Enzym für die Synthese von Testosteron (17--Hydroxylase, C17,20-Lyase). Da das Enzym auch den Mineralkortikoidhaushalt beeinflusst wird die Therapie mit Prednison kombiniert. Im Gegensatz zu den LHRH-Agonsiten und-Antagonisten wird nicht nur die testikuläre, sondern auch die adrenale und die intratumorale Androgensynthese blockiert. Abiraterone ist sowohl in der Therapie vor als auch nach Docetaxel Chemotherapie zugelassen. Dies beruht auf einem signifikant verlängertem Intervall der Progression als auch einem signifikanten Überlebensvorteil in 2 großen Phase III Studien. Die Nebenwirkungen sind moderat. Im Vordergrund stehen Ödemneigung, Hypokaliämien und Bluthochdruck.
MDV3100
MDV3100 zählt zu den sogenannten next generation Androgenrezeptorblockern. Im Gegensatz zu Bicalutamid ist die antiandrogene Wirkung nicht nur auf eine Blockade des Androgenrezeptors beschränkt. Es liegt zusätzlich eine Hemmung der intranukleären Translokation des AR-Komplex und Hemmung der DNA-Bindung des AR-Komplexes vor. Ähnlich wie Abiraterone konnte MDV 3100 nahezu zeitgleich einen signifikanten Vorteil in Bezug auf Progression und Überleben der Patienten erbringen.
Häufige Nebenwirkungen waren Fatigue, Diarrhö, hot flush, Muskel- und Kopfschmerzen. Unter der Medikation wurden in geringem Ausmaß Epilepsien beschrieben, so dass bei bekannter Anamnese ein Einsatz von Enzalutamid nicht empfohlen wird.
Radium-223
Eine Radionuklidtherapie war bisher mit einer hohen Hämatotoxizität vergesellschaftet. Patienten waren hiernach häufig einer weiteren zytotoxischen Therapie nicht mehr zugänglich. Radium-223-dichlorid ist ein Alpha-Strahler der in der Therapie des symptomatischen ossär metastasierten kastrationsresistenten Prostatakarzinoms zugelassen ist. Im Gegensatz zu den zuvor üblichen Beta-Strahlern konnte das Radium-223 der placebokontrollierten Phase-III-Studie ALSYMPCA zu den signifikanten Vorteilen in der Symptomreduktion erstmals auch eine Verlängerung des Gesamtüberlebens erzielen. Bei einer sehr kurzen Reichweite von < 100 μm ist auch die Auswirkung auf das angrenzende gesunde Knochenmark und damit die Hämatotoxizität gering. Im Vordergrund der Nebenwirkungen stehen eine Thrombopenie und gastrointestinale Nebenwirkungen wie Diarrhoe und Übelkeit. Die Therapie beschränkt sich derzeit auf ossär metastasierte Patienten mit Lymphkotenmetastasen <3cm ohne viszerale Metastasen. Eine Kombinationstherapie bei insgesamt wenig Nebenwirkungen ist möglich aber aktuell ausserhalb der Zulassung. Diesbezüglich laufen klinische Studien.
Mit der Verfügbarkeit verschiedener Therapieoptionen im kastrationsresistenten Tumorstadium ergibt sich zwangsläufig die Frage nach der idealen Sequenz nach Erstlinie. Insgesamt ist die Datenlage hierzu noch eingeschränkt. Aus retrospektiv generierten Daten konnten allerdings einige Erkenntnisse gewonnen werden:
- die primär eingeleitete Therapie hat meist das beste Therapieansprechen
- die Sequenz Hormonmanipulation gefolgt von Hormonmanipulation ist mit nur einem geringen Ansprechen assoziiert
- Cabazitaxel hat auch in der letzten Linie ein günstiges Therapieansprechen
In einer Zusammenfassung der vorhandenen Studien konnte gezeigt werden, dass die Patienten, die in den durchlaufenen Sequenzen eine 2. Linien Chemotherapie erhalten hatten insgesamt ein günstigeres Outcome im Vergleich zu Patienten hatten, die lediglich weiteren Hormonmanipulationen zugeführt wurden. Entscheidend ist ein enges Therapiemonitoring, um den Patienten möglichst alle verfügbaren Therapien bei Progress anbieten zu können.
Ab dem kastrationsresistenten Tumorstadium ist von den nationalen und internationalen Leitlinien eine Gabe von Bisphosphonaten oder Rank-L-Antagonisten empfohlen. Bei beiden Präparaten konnte eine signifikante Verlängerung des Intervalls bis zum Auftreten eines skeletalen Ereignisses nachgewiesen werden. Beide Präparate sollen mit einer Kalzium und Vit-D Substitution kombiniert werden. Bei potentiellen Nebenwirkungen, hervorzuheben sind insbesondere schwerwiegende Nebenwirkungen wie die Ausbildung einer aseptischen Kiefernekrose oder einer Niereninsuffizienz ist die Indikation zur Applikation streng an die Zulassung zu stellen. Der Effekt beschränkt sich auf das kastrationsresistente Tumorstadium, so dass eine zu frühe Applikation lediglich mit der Gefahr der Entwicklung von Nebenwirkungen assoziiert ist.
Einen Überblick über alle klinischen Studien zum Prostatakarzinom finden Sie in unserem Studienregister.
![[Bildbeschreibung]](https://webstatic.uk-koeln.de/im/headerimage/166450/standard/820/image-166450.png)
![[Bildbeschreibung]](https://webstatic.uk-koeln.de/im/headerimage/166448/standard/820/image-166448.png)
![[Bildbeschreibung]](https://webstatic.uk-koeln.de/im/headerimage/166449/standard/820/image-166449.png)
![[Bildbeschreibung]](https://webstatic.uk-koeln.de/im/headerimage/166451/standard/820/image-166451.png)
![[Bildbeschreibung]](https://webstatic.uk-koeln.de/im/gallery/166450/image/thumb/image-166450.png)
![[Bildbeschreibung]](https://webstatic.uk-koeln.de/im/gallery/166448/image/thumb/image-166448.png)
![[Bildbeschreibung]](https://webstatic.uk-koeln.de/im/gallery/166449/image/thumb/image-166449.png)
![[Bildbeschreibung]](https://webstatic.uk-koeln.de/im/gallery/166451/image/thumb/image-166451.png)